Sommario per questo articolo:
1. Sviluppo di aminoacidi
2. Proprietà strutturali
3. Composizione chimica
4. Classificazione
5. Sintesi
6. Proprietà fisico -chimiche
7. Tossicità
8. Attività antimicrobica
9. Proprietà reologiche
10. Applicazioni nel settore cosmetico
11. Applicazioni nei cosmetici di tutti i giorni
Aminoacidi tensioattivi (AAS)sono una classe di tensioattivi formati combinando gruppi idrofobici con uno o più aminoacidi. In questo caso, gli aminoacidi possono essere sintetici o derivati da idrolizzati proteici o fonti rinnovabili simili. Questo documento copre i dettagli della maggior parte delle rotte sintetiche disponibili per AAS e l'effetto di percorsi diversi sulle proprietà fisico -chimiche dei prodotti finali, tra cui solubilità, stabilità della dispersione, tossicità e biodegradabilità. Come classe di tensioattivi nella crescente domanda, la versatilità degli AA grazie alla loro struttura variabile offre un gran numero di opportunità commerciali.
Dato che i tensioattivi sono ampiamente utilizzati in detergenti, emulsionanti, inibitori della corrosione, recupero di petrolio terziario e prodotti farmaceutici, i ricercatori non hanno mai smesso di prestare attenzione ai tensioattivi.
I tensioattivi sono i prodotti chimici più rappresentativi che vengono consumati in grandi quantità su base giornaliera in tutto il mondo e hanno avuto un impatto negativo sull'ambiente acquatico.Gli studi hanno dimostrato che l'uso diffuso dei tensioattivi tradizionali può avere un impatto negativo sull'ambiente.
Oggi la non tossicità, la biodegradabilità e la biocompatibilità sono quasi importanti per i consumatori quanto l'utilità e le prestazioni dei tensioattivi.
I biosurfattanti sono tensioattivi sostenibili ecologici che sono naturalmente sintetizzati da microrganismi come batteri, funghi e lievito o secreti extracellular.Pertanto, i biosurfattanti possono anche essere preparati dal design molecolare per imitare le strutture anfifiliche naturali, come fosfolipidi, alchil glicosidi e aminoacidi acilici.
Aminoacidi tensioattivi (AAS)sono uno dei tensioattivi tipici, generalmente prodotti da materie prime di derivazione animale o agricola. Negli ultimi due decenni, AAS ha attirato molto interesse da parte degli scienziati come nuovi tensioattivi, non solo perché possono essere sintetizzati da risorse rinnovabili, ma anche perché gli AA sono prontamente degradabili e hanno sottoprodotti innocui, rendendoli più sicuri per l'ambiente.
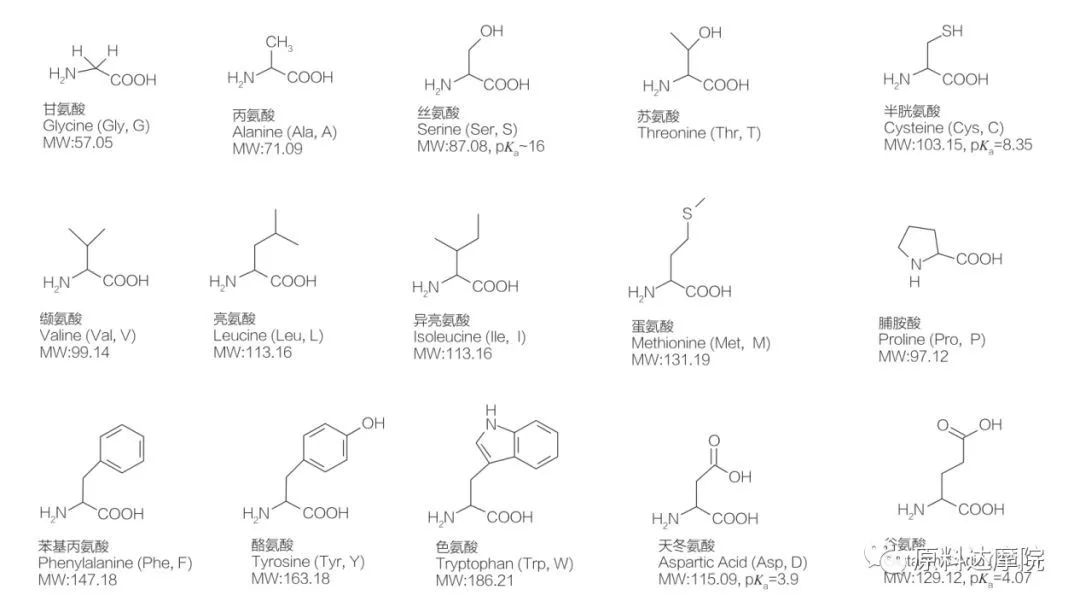
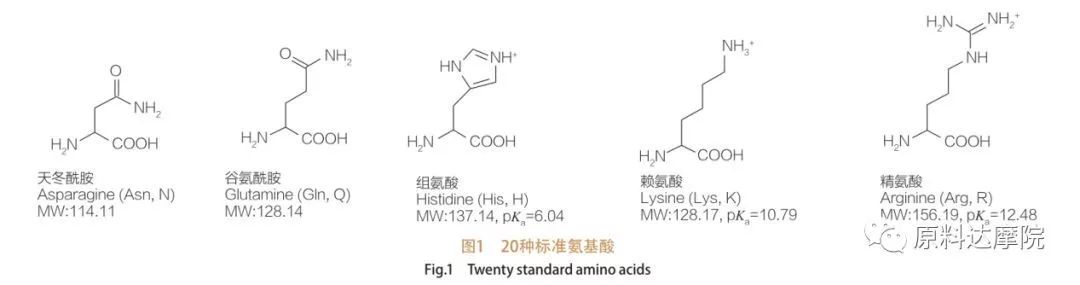
L'AAS può essere definito come una classe di tensioattivi costituiti da aminoacidi contenenti gruppi di aminoacidi (HO 2 C-CHR-NH 2) o residui di aminoacidi (HO 2 C-CHR-NH-). Le 2 regioni funzionali di aminoacidi consentono la derivazione di un'ampia varietà di tensioattivi. Un totale di 20 aminoacidi proteinogenici standard esistono in natura e sono responsabili di tutte le reazioni fisiologiche nelle attività di crescita e vita. Differiscono l'uno dall'altro solo in base al residuo R (Figura 1, Pk A è il logaritmo negativo della costante di dissociazione acida della soluzione). Alcuni sono non polari e idrofobici, alcuni sono polari e idrofili, alcuni sono di base e altri sono acidi.
Poiché gli aminoacidi sono composti rinnovabili, i tensioattivi sintetizzati dagli aminoacidi hanno anche un alto potenziale per diventare sostenibili e rispettosi dell'ambiente. La struttura semplice e naturale, la bassa tossicità e la rapida biodegradabilità spesso li rendono superiori ai tensioattivi convenzionali. Utilizzando materie prime rinnovabili (ad es. Aminoacidi e oli vegetali), AAS può essere prodotto da diverse rotte biotecnologiche e rotte chimiche.
All'inizio del XX secolo, gli aminoacidi sono stati scoperti per la prima volta come substrati per la sintesi dei tensioattivi.Gli AA sono stati utilizzati principalmente come conservanti nelle formulazioni farmaceutiche e cosmetiche.Inoltre, gli AA sono risultati biologicamente attivi contro una varietà di batteri, tumori e virus che causano la malattia. Nel 1988, la disponibilità di AA a basso costo ha generato interesse di ricerca per l'attività superficiale. Oggi, con lo sviluppo della biotecnologia, alcuni aminoacidi possono anche essere sintetizzati commercialmente su larga scala per lievito, il che dimostra indirettamente che la produzione di AAS è più rispettosa dell'ambiente.
01 Sviluppo di aminoacidi
All'inizio del XIX secolo, quando furono scoperti per la prima volta gli aminoacidi naturali, le loro strutture erano estremamente preziose, utilizzabili come materie prime per la preparazione di anfifili. Il primo studio sulla sintesi di AAS è stato riportato da Bondi nel 1909.
In quello studio, la N-acilglicina e la N-acilalanina sono state introdotte come gruppi idrofili per i tensioattivi. Il lavoro successivo prevedeva la sintesi di lipoaminoacidi (AAS) usando glicina e alanina e Hentrich et al. ha pubblicato una serie di risultati,Compresa la prima applicazione di brevetto, sull'uso di sali di sarcosinato acile e aspartato acilico come tensioattivi nei prodotti per la pulizia della casa (ad es. shampoo, detergenti e stuoierghi).Successivamente, molti ricercatori hanno studiato la sintesi e le proprietà fisico -chimiche degli aminoacidi acilici. Ad oggi, è stato pubblicato un ampio corpus di letteratura su sintesi, proprietà, applicazioni industriali e biodegradabilità di AAS.
02 Proprietà strutturali
Le catene di acidi grassi idrofobici non polari di AAS possono variare in struttura, lunghezza della catena e numero.La diversità strutturale e l'elevata attività superficiale di AAS spiegano la loro ampia diversità compositiva e proprietà fisico -chimiche e biologiche. I gruppi di testa di AA sono composti da aminoacidi o peptidi. Le differenze nei gruppi di testa determinano l'adsorbimento, l'aggregazione e l'attività biologica di questi tensioattivi. I gruppi funzionali nel gruppo della testa determinano quindi il tipo di AAS, inclusi cationici, anionici, non ionici e anfoterici. La combinazione di aminoacidi idrofili e porzioni idrofobiche a catena lunga formano una struttura anfifilica che rende attiva la molecola attivo. Inoltre, la presenza di atomi di carbonio asimmetrici nella molecola aiuta a formare molecole chirali.
03 Composizione chimica
Tutti i peptidi e i polipeptidi sono i prodotti di polimerizzazione di questi quasi 20 α-aminoacidi-proteinogeni. Tutti i 20 α-aminoacidi contengono un gruppo funzionale dell'acido carbossilico (-COOH) e un gruppo funzionale amminico (-NH 2), entrambi attaccati allo stesso atomo α-carbonio tetraedrico. Gli aminoacidi differiscono l'uno dall'altro dai diversi gruppi R attaccati al carbonio α (ad eccezione della licina, dove il gruppo R è idrogeno.) I gruppi R possono differire in struttura, dimensione e carica (acidità, alcalinità). Queste differenze determinano anche la solubilità degli aminoacidi in acqua.
Gli aminoacidi sono chirali (ad eccezione della glicina) e sono otticamente attivi per natura perché hanno quattro diversi sostituenti legati al carbonio alfa. Gli aminoacidi hanno due possibili conformazioni; Sono immagini non specchietti reciproche, nonostante il fatto che il numero di L-Stereoisomer sia significativamente più alto. Il gruppo R presente in alcuni aminoacidi (fenilalanina, tirosina e triptofano) è aril, portando a un assorbimento UV massimo a 280 nm. L'α-COOH acido e l'α-NH di base negli aminoacidi sono in grado di ionizzazione, ed entrambi gli stereoisomeri, a seconda di quale siano, costruiscono l'equilibrio di ionizzazione mostrato di seguito.
R-cooh ↔r-coo-+ h+
R-NH3+↔r-nh2+ h+
Come mostrato nell'equilibrio di ionizzazione sopra, gli aminoacidi contengono almeno due gruppi debolmente acidi; Tuttavia, il gruppo carbossilico è molto più acido rispetto al gruppo amminico protonato. pH 7.4, il gruppo carbossilico viene deprotonato mentre il gruppo amminico è protonato. Gli aminoacidi con gruppi R non ionizzabili sono elettricamente neutri a questo pH e formano zwitterion.
04 Classificazione
Gli AA possono essere classificati in base a quattro criteri, che sono descritti di seguito a turno.
4.1 in base all'origine
| Secondo l'origine, AAS può essere diviso in 2 categorie come segue. ① Categoria naturale Alcuni composti presenti in natura contenenti aminoacidi hanno anche la capacità di ridurre la tensione di superficie/interfacciale e alcuni persino superano l'efficacia dei glicolipidi. Questi AA sono anche noti come lipopeptidi. I lipopeptidi sono composti a basso peso molecolare, generalmente prodotti dalle specie di Bacillus.
Tali AA sono ulteriormente divisi in 3 sottoclassi:Surfagin, iturin e fengycin.
|
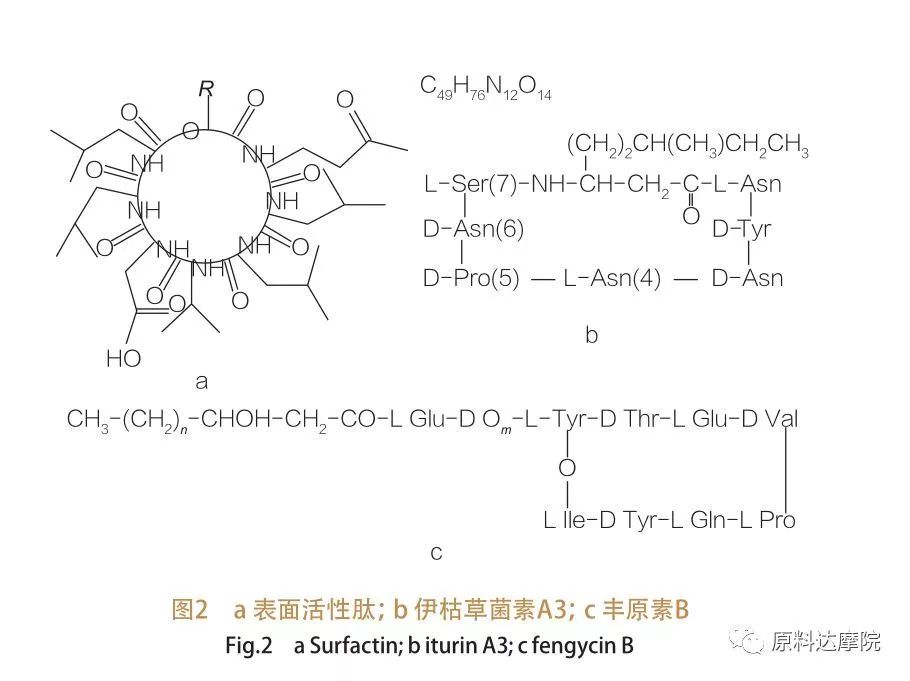
| La famiglia di peptidi attivo superficiale comprende varianti di eptapeptidi di una varietà di sostanze,Come mostrato nella Figura 2A, in cui una catena di acidi grassi β-idrossi insaturi C12-C16 è collegata al peptide. Il peptide attivo superficiale è un latino macrociclico in cui l'anello è chiuso dalla catalisi tra il C-terminus dell'acido grasso β-idrossi e il peptide. Nella sottoclasse di iturin, ci sono sei varianti principali, vale a dire iturin A e C, micosubtilina e bacillomicina D, F e L.In tutti i casi, gli eptapeptidi sono legati alle catene C14-C17 di acidi grassi β-amino (le catene possono essere diverse). Nel caso degli ekurimicine, il gruppo aminoaggio nella posizione β può formare un legame ammidico con il terminale C formando così una struttura macrociclica di lattamme.
La fengicina sottoclasse contiene la fengycin A e B, che sono anche chiamate plapastatina quando Tyr9 è configurato da D.Il decapeptide è collegato a una catena di acidi grassi β -idrossi saturi o insaturi C14 -C18. Strutturalmente, la plapastatina è anche un latino macrociclico, contenente una catena laterale Tyr nella posizione 3 della sequenza peptidica e forma un legame estere con il residuo C-terminale, formando così una struttura ad anello interna (come è nel caso di molti lipopeptidi Pseudomonas).
② categoria sintetica L'AAS può anche essere sintetizzato usando uno qualsiasi degli aminoacidi acidi, di base e neutri. Gli aminoacidi comuni usati per la sintesi di AA sono acido glutammico, serina, prolina, acido aspartico, glicina, arginina, alanina, leucina e idrolizzati proteici. Questa sottoclasse di tensioattivi può essere preparata con metodi chimici, enzimatici e chemioenzimatici; Tuttavia, per la produzione di AAS, la sintesi chimica è più economicamente fattibile. Esempi comuni includono l'acido N-lauroil-L-glutammico e l'acido N-Palmitoil-L-glutamico.
|
4.2 Basato sui sostituenti della catena alifatica
Sulla base dei sostituenti della catena alifatica, i tensioattivi a base di aminoacidi possono essere divisi in 2 tipi.
Secondo la posizione del sostituente
| AAS sostituito Nei composti sostituiti a N, un gruppo amminico viene sostituito da un gruppo lipofilo o da un gruppo carbossilico, risultando in una perdita di basicità. L'esempio più semplice di AAS sostituito da N sono gli aminoacidi N-acil, che sono essenzialmente tensioattivi anionici. Gli AA sostituiti da N hanno un legame ammidico attaccato tra le porzioni idrofobiche e idrofile. Il legame ammidico ha la capacità di formare un legame idrogeno, che facilita il degrado di questo tensioattivo in un ambiente acido, rendendolo così biodegradabile.
AAS sostituito da C Nei composti sostituiti in C, la sostituzione si verifica nel gruppo carbossilico (tramite un legame ammide o estere). I composti tipici sostituiti a C (esteri o ammidi) sono essenzialmente tensioattivi cationici.
③n- e c-sostituito AAS In questo tipo di tensioattivo, entrambi i gruppi amino e carbossilici sono la parte idrofila. Questo tipo è essenzialmente un tensioattivo anfoterico. |
4.3 in base al numero di code idrofobiche
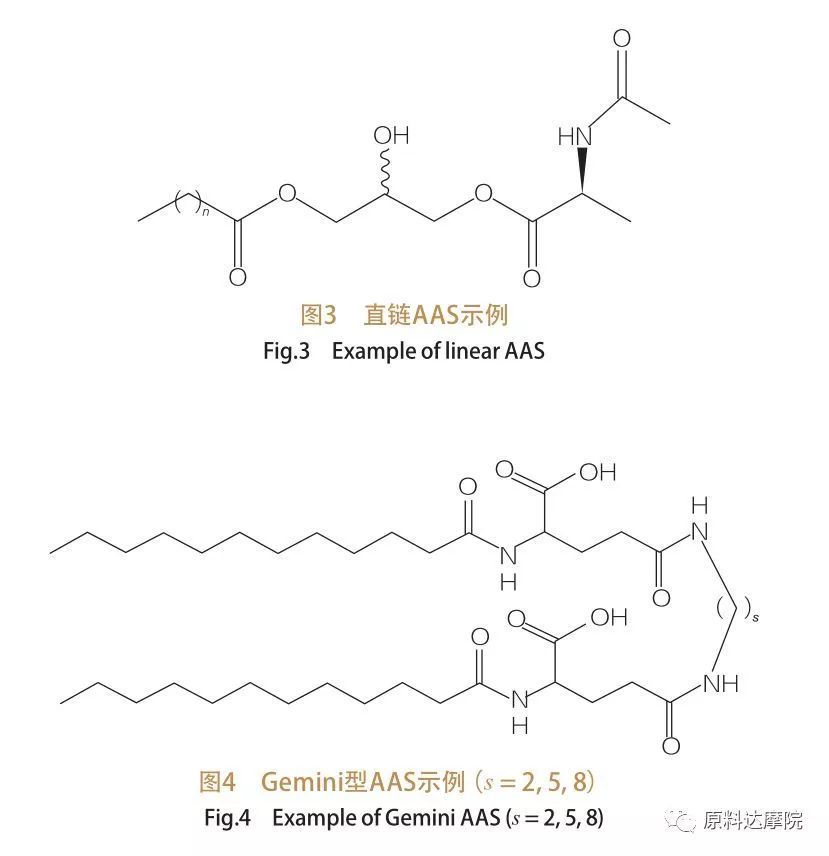
Sulla base del numero di gruppi di testa e code idrofobiche, AAS può essere diviso in quattro gruppi. AAS a catena dritta, tipo AAS GEMINI (dimero), tipo glicerolipido AAS e AA AAS anfifilico bicefalico (BOLA). I tensioattivi a catena dritta sono tensioattivi costituiti da aminoacidi con solo una coda idrofobica (Figura 3). I gemelli di tipo AA hanno due gruppi di testa polare aminoacidi e due code idrofobiche per molecola (Figura 4). In questo tipo di struttura, i due AA a catena dritta sono collegati da un distanziatore e sono quindi chiamati dimeri. Nel tipo glicerolipido AAS, d'altra parte, le due code idrofobiche sono attaccate allo stesso gruppo di testa di aminoacidi. Questi tensioattivi possono essere considerati analoghi di monogliceridi, digliceridi e fosfolipidi, mentre in AAS di tipo Bola, due gruppi di testa di aminoacidi sono collegati da una coda idrofobica.
4.4 in base al tipo di gruppo di testa
①Cationic AAS
Il gruppo principale di questo tipo di tensioattivo ha una carica positiva. Il primo AA cationico è l'arginato di cocoil etilico, che è un carbossilato di pirrolidone. Le proprietà uniche e diverse di questo tensioattivo lo rendono utile in disinfettanti, agenti antimicrobici, agenti antistatici, balsami per capelli, oltre ad essere delicati sugli occhi e sulla pelle e facilmente biodegradabili. Singare e Mhatre hanno sintetizzato AA Cationic a base di arginina e hanno valutato le loro proprietà fisico-chimiche. In questo studio, hanno rivendicato alti rendimenti dei prodotti ottenuti utilizzando le condizioni di reazione di Schotten-Baumann. Con l'aumentare della lunghezza della catena alchilica e dell'idrofobicità, si è scoperto che l'attività superficiale del tensioattivo aumenta e la concentrazione critica delle micelle (CMC) a diminuire. Un altro è la proteina acilica quaternaria, che è comunemente usata come balsamo nei prodotti per la cura dei capelli.
② AAS AAS
Nei tensioattivi anionici, il gruppo polare della testa del tensioattivo ha una carica negativa. La sarcosina (CH 3 -NH -CH 2 -CoOH, N -metilglicina), un aminoacido comunemente presente nei ricci di mare e nelle stelle marine, è chimicamente correlato alla glicina (NH 2 -Ch 2 -Cooh,), un aminoacido di base che si trova nelle cellule dei mammiferi. -Cooh,) è chimicamente correlato alla glicina, che è un aminoacido di base che si trova nelle cellule di mammifero. L'acido laurico, l'acido tetradecanoico, l'acido oleico e i loro alogenuri ed esteri sono comunemente usati per sintetizzare i tensioattivi sarcosinati. I sarcosinati sono intrinsecamente delicati e sono quindi comunemente usati in collutori, shampoo, schiume a rasatura a spruzzo, creme solari, detergenti per la pelle e altri prodotti cosmetici.
Altri AA anionici disponibili in commercio includono AMisoft CS-22 e AmiliteGCK-12, che sono nomi commerciali per il sodio-cocoil-L-glutammato e il glicinato N-cocoily di potassio, rispettivamente. L'amilite è comunemente usata come agente schiumoso, detergente, solubilizzatore, emulsionante e disperdente e ha molte applicazioni in cosmetici, come shampoo, saponi da bagno, lavaggi del corpo, dentifogli, detergenti per il viso, saponi per la pulizia, detergenti di lenti a contatto e tensiottanti domestici. Amisoft viene utilizzato come un lieve detergente per la pelle e i capelli, principalmente nei detergenti per il viso e del corpo, i detergenti sintetici a blocchi, i prodotti per la cura del corpo, gli shampoo e altri prodotti per la cura della pelle.
③zwitterionic o anfoterico AAS
I tensioattivi anfoterici contengono siti sia acidi che di base e possono quindi cambiare la loro carica modificando il valore del pH. Nei media alcalini si comportano come tensioattivi anionici, mentre in ambienti acidi si comportano come tensioattivi cationici e in mezzi neutri come i tensioattivi anfoterici. Lauril lisina (LL) e alcossia (2-idrossipropil) arginina sono gli unici tensioattivi anfoteri noti basati su aminoacidi. LL è un prodotto di condensazione di lisina e acido laurico. A causa della sua struttura anfoterica, LL è insolubile in quasi tutti i tipi di solventi, ad eccezione di solventi molto alcalini o acidi. Come polvere organica, LL ha un'eccellente adesione alle superfici idrofile e un basso coefficiente di attrito, dando a questo tensioattivo eccellente capacità di lubrificazione. LL è ampiamente utilizzato nelle creme per la pelle e nei balsami per capelli ed è anche usato come lubrificante.
④nonionic AAS
I tensioattivi non ionici sono caratterizzati da gruppi di testa polare senza cariche formali. Otto nuovi tensioattivi non ionici etossilati sono stati preparati da al-Sabagh et al. da α-aminoacidi solubili in olio. In questo processo, la L-fenilalanina (LEP) e la L-leucina sono state prima esterificate con esadecanolo, seguite da amidazione con acido palmitico per dare due ammidi e due esteri di α-aminoacidi. Le ammidi e gli esteri hanno quindi subito reazioni di condensazione con ossido di etilene per preparare tre derivati di fenilalanina con un numero diverso di unità di poliossietilene (40, 60 e 100). Si è scoperto che questi AA non ionici avevano una buona determinazione e proprietà di schiuma.
05 Sintesi
5.1 Percorso sintetico di base
In AAS, i gruppi idrofobici possono essere attaccati a siti di acido amminico o carbossilico o attraverso le catene laterali degli aminoacidi. Sulla base di questo, sono disponibili quattro percorsi sintetici di base, come mostrato nella Figura 5.
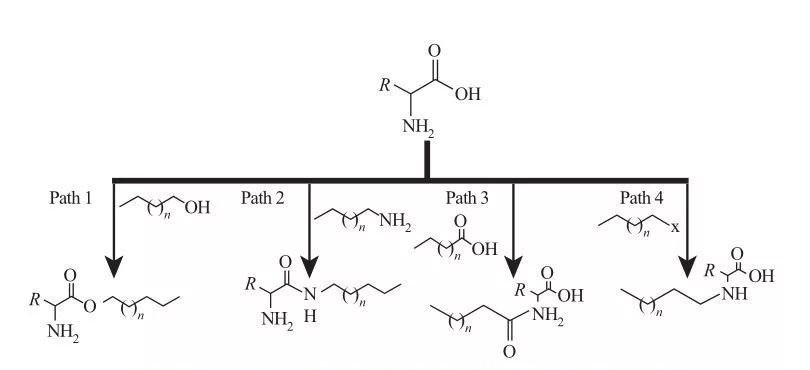
Fig.5 percorsi di sintesi fondamentali dei tensioattivi a base di aminoacidi
| Pathway 1. Le amine estere anfifiliche sono prodotte dalle reazioni di esterificazione, nel qual caso la sintesi del tensioattivo è generalmente raggiunta mediante riflusso di alcoli grassi e aminoacidi in presenza di un agente disidratante e un catalizzatore acido. In alcune reazioni, l'acido solforico agisce sia come catalizzatore che come agente disidratante.
Pathway 2. Gli aminoacidi attivati reagiscono con alchilammine per formare legami ammidri, con conseguente sintesi di amidoamine anfifiliche.
Pathway 3. Gli acidi di amido sono sintetizzati reagendo i gruppi amminici di aminoacidi con acidi amido.
Pathway 4. Gli aminoacidi alchilici a catena lunga sono stati sintetizzati dalla reazione di gruppi di ammina con aloalcani. |
5.2 Progressi nella sintesi e nella produzione
5.2.1 Sintesi di tensioattivi aminoacidi/peptidi a catena singola
Gli aminoacidi N-acil o O-acil o peptidi possono essere sintetizzati mediante acilazione catalizzata da enzima di gruppi di ammina o idrossile con acidi grassi. Il primo rapporto sulla sintesi catalizzata dalla lipasi priva di solventi di derivati aminoacidi di amminoacidi o metil estere ha usato Candida Antartide, con rese che vanno dal 25% al 90% a seconda dell'amminoacido target. Anche il metil etil chetone è stato usato come solvente in alcune reazioni. Vonderhagen et al. Descritto anche le reazioni di N-acilazione catalizzate dalla lipasi e proteasi di aminoacidi, idrolizzati di proteine e/o loro derivati usando una miscela di acqua e solventi organici (ad es. Dimetilformamide/acqua) e metil e ketone.
All'inizio, il problema principale con la sintesi catalizzata da enzimi di AAS era le rese basse. Secondo Valivety et al. La resa dei derivati degli aminoacidi N-tetradecanoil era solo del 2% -10% anche dopo aver utilizzato lipasi diverse e incubazione a 70 ° C per molti giorni. Montet et al. Ha anche riscontrato problemi relativi alla bassa resa degli aminoacidi nella sintesi della lisina N-acil usando acidi grassi e oli vegetali. Secondo loro, la resa massima del prodotto era del 19% in condizioni prive di solventi e utilizzando solventi organici. Lo stesso problema è stato riscontrato da Valivety et al. Nella sintesi di derivati di metil estere N-CBZ-L-lisina o N-CBZ-lisina.
In questo studio, hanno affermato che la resa di 3-O-tetradecanoyl-L-serina era dell'80% quando si utilizzava serina protetta da N come substrato e Novozyme 435 come catalizzatore in un ambiente fuso senza solventi. Nagao e Kito hanno studiato l'O-acilazione di L-serina, L-omoserina, L-treonina e l-tirosina (let) quando usavano la lipasi i risultati della reazione (la lipasi era ottenuta da candida cilindracea e lizopus detemar Acilazione di L-treonina e lasciato che si è verificato.
Molti ricercatori hanno supportato l'uso di substrati economici e prontamente disponibili per la sintesi di AA economici. Soo et al. ha affermato che la preparazione di tensioattivi a base di olio di palma funziona meglio con lipoenzima immobilizzato. Hanno notato che la resa dei prodotti sarebbe migliore nonostante la reazione che richiede tempo (6 giorni). Gerova et al. ha studiato la sintesi e l'attività superficiale di N-Palmitoil AAS chiral basato su metionina, prolina, leucina, treonina, fenilalanina e fenilglicina in una miscela ciclica/racemica. Pang e Chu hanno descritto la sintesi di monomeri a base di aminoacidi e monomeri a base di acido dicarbossilico in soluzione Una serie di esteri di poliammide a base di aminoacidi funzionali e biodegradabili sono stati sintetizzati da reazioni di co-condensazione in soluzione.
Cantaeuzene e Guerreiro hanno riportato l'esterificazione di gruppi di acido carbossilico di BOC-Ala-OH e BOC-ASP-OH con alcoli e dioli alifatici a catena lunga, con diclorometano come solvente e agarosio 4b (sefarosio 4b) come caduta. In questo studio, la reazione di BOC-Ala-OH con alcoli grassi fino a 16 carboni ha dato buoni rendimenti (51%), mentre per BOC-ASP-OH 6 e 12 carboni erano migliori, con una resa corrispondente del 63% [64]. 99,9%) in rendimenti che vanno dal 58%al 76%, che sono stati sintetizzati dalla formazione di legami ammidici con vari alchilammine a catena lunga o legami estere con alcoli grassi da parte di CBZ-Arg-Ome, dove la Papaina ha agito come catalizzatore.
5.2.2 Sintesi di tensioattivi di aminoacidi/peptidi a base di gemelli
I tensioattivi di gemelli a base di aminoacidi sono costituiti da due molecole AAS a catena dritta collegate testa a testa tra loro da un gruppo distanziatore. Esistono 2 possibili schemi per la sintesi chemioenzimatica di tensioattivi a base di aminoacidi di tipo gemini (Figure 6 e 7). Nella Figura 6, 2 derivati di aminoacidi vengono reagiti con il composto come gruppo distanziatore e quindi vengono introdotti 2 gruppi idrofobici. Nella Figura 7, le 2 strutture a catena dritta sono direttamente collegate da un gruppo di distanziali bifunzionali.
Il primo sviluppo della sintesi catalizzata dagli enzimi di lipoaminoacidi Gemini è stato aperto da Valivety et al. Yoshimura et al. ha studiato la sintesi, l'adsorbimento e l'aggregazione di un tensioattivo di gemelli a base di aminoacidi basato sul bromuro di cistina e N-alchile. I tensioattivi sintetizzati sono stati confrontati con i corrispondenti tensioattivi monomerici. Faustino et al. ha descritto la sintesi di AA monomerici basati su urea anionica basati su L-cistina, D-cistina, DL-cistina, L-cisteina, L-metionina e L-solfolanina e le loro coppie di gemelli mediante conduttività, tensione di superficie di equilibrio e caratterizzazione fluorescente stabile. È stato dimostrato che il valore CMC dei Gemelli era più basso confrontando monomero e Gemelli.
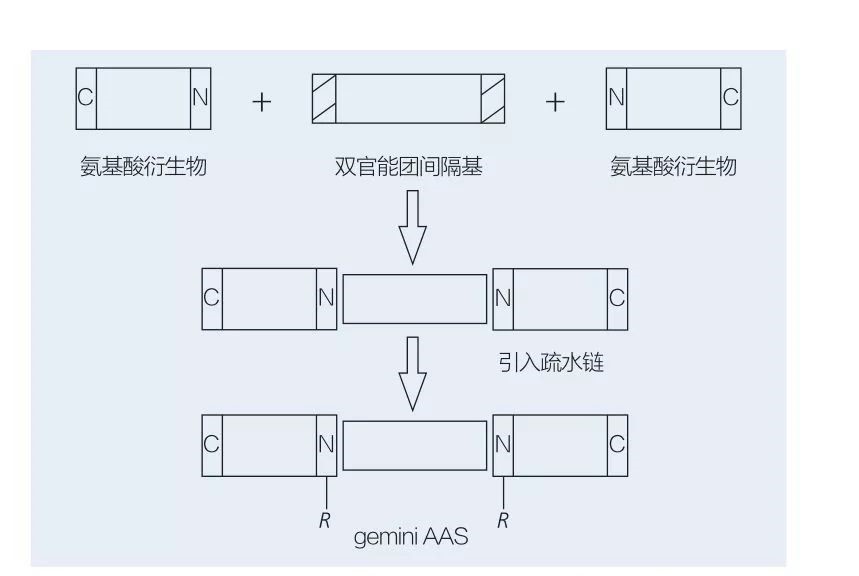
Fig.6 Sintesi di Gemini AAs usando derivati e distanziali AA, seguiti dall'inserimento del gruppo idrofobico
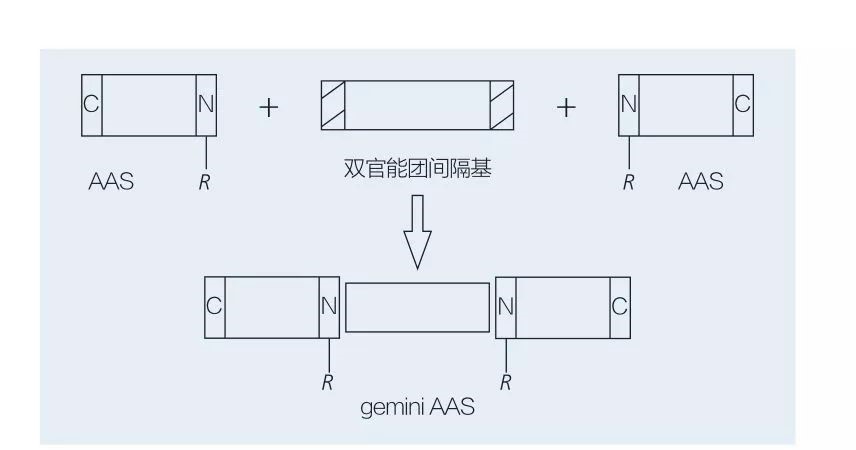
Fig.7 Sintesi di Gemini AASS usando distanziatore bifunzionale e AAS
5.2.3 Sintesi di tensioattivi glicerolipidi di aminoacidi/peptidi
I tensioattivi di aminoacidi/peptidi glicerolipidi sono una nuova classe di aminoacidi lipidici che sono analoghi strutturali di glicerolo mono- (o di-) esteri e fosfolipidi, a causa della loro struttura di una o due catene grasse con un aminoacido collegato al ghiorno del glicerolo da un legame estere. La sintesi di questi tensioattivi inizia con la preparazione di esteri di glicerolo di aminoacidi a temperature elevate e in presenza di un catalizzatore acido (ad es. BF 3). Anche la sintesi catalizzata dagli enzimi (usando idrolasi, proteasi e lipasi come catalizzatori) è una buona opzione (Figura 8).
È stata segnalata la sintesi catalizzata dagli enzimi di coniugati di gliceridi di arginina dilaurilato usando la papaina. Sono state anche segnalate sintesi di coniugati di estere di diacilglicerolo dall'acetilarginina e valutazione delle loro proprietà fisico -chimiche.
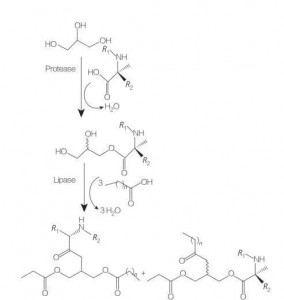
Fig.8 Sintesi di coniugati di aminoacidi mono e diacilglicerolo
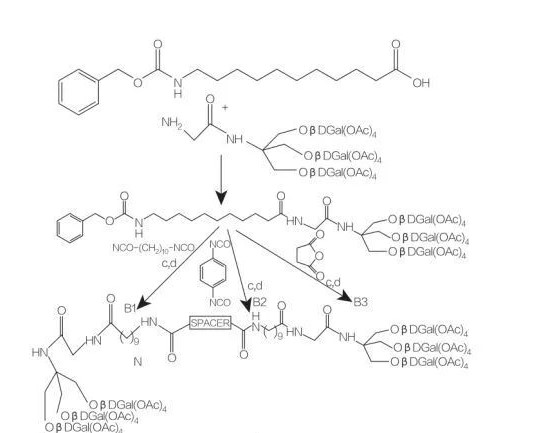
Spacer: NH- (Ch2)10-Nh: compostoB1
Spacer: NH-C6H4-Nh: compostoB2
Spacer: Ch2-Ch2: compostoB3
Fig.9 Sintesi di anfifili simmetrici derivati da tris (idrossimetil) aminometano
5.2.4 Sintesi di tensioattivi di aminoacidi/peptidi a base di Bola
Gli anfifili di tipo Bola a base di aminoacidi contengono 2 aminoacidi collegati alla stessa catena idrofobica. Franceschi et al. ha descritto la sintesi di anfifili di tipo Bola con 2 aminoacidi (d o l-alanina o L-istidina) e 1 catena alchilica di diverse lunghezze e hanno studiato la loro attività superficiale. Discutono la sintesi e l'aggregazione di nuovi anfifili di tipo Bola con una frazione di aminoacido (usando un β-aminoacido non comune o un alcol) e un gruppo di distanziali C12 -C20. I non comuni β-aminoacidi utilizzati possono essere un aminoacide di zucchero, un aminoacido derivato dall'azidotimin (AZT), un aminoacido norbornene e un alcol aminoto derivato da AZT (Figura 9). La sintesi di anfifili simmetrici di tipo Bola derivati da Tris (idrossimetil) aminometano (Tris) (Figura 9).
06 Proprietà fisico -chimiche
È noto che i tensioattivi a base di aminoacidi (AAS) sono diversi e versatili di natura e hanno una buona applicabilità in molte applicazioni come una buona solubilizzazione, buone proprietà di emulsificazione, elevata efficienza, elevata prestazione di attività superficiale e buona resistenza alle acque dure (tolleranza a ioni di calcio).
Sulla base delle proprietà del tensioattivo degli aminoacidi (ad es. Tensione superficiale, CMC, comportamento di fase e temperatura di Krafft), sono state raggiunte le seguenti conclusioni dopo ampie studi: l'attività superficiale di AAS è superiore a quella della sua controparte di tensioattivo convenzionale.
6.1 Concentrazione critica delle micelle (CMC)
La concentrazione critica di micelle è uno dei parametri importanti dei tensioattivi e governa molte proprietà attive di superficie come la solubilizzazione, la lisi cellulare e la sua interazione con i biofilm, ecc. In generale, aumentando la lunghezza della catena della coda idrocarburica (aumento dell'idrofobicità) porta a una diminuzione del valore CMC della soluzione di tensiottico, aumentando così l'attività superficiale. I tensioattivi basati su aminoacidi di solito hanno valori di CMC più bassi rispetto ai tensioattivi convenzionali.
Attraverso diverse combinazioni di gruppi di testa e code idrofobiche (ammide mono-cationica, ammide bi-cationica, estere a base di ammide bi-cationica), Infante et al. sintetizzato tre AA a base di arginina e studiato il loro CMC e γCMC (tensione superficiale a CMC), dimostrando che i valori CMC e γCMC sono diminuiti con l'aumentare della lunghezza della coda idrofobica. In un altro studio, Singare e Mhatre hanno scoperto che il CMC dei tensioattivi N-α-acilarginina è diminuita con l'aumentare del numero di atomi di carbonio a coda idrofobica (Tabella 1).
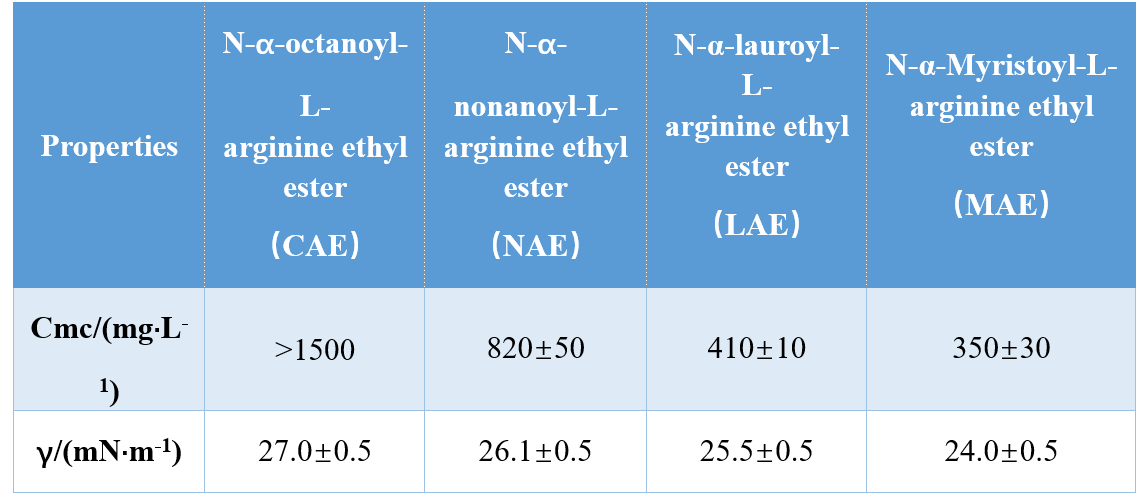
Yoshimura et al. ha studiato la CMC dei tensioattivi di gemelli a base di aminoacidi derivati dalla cisteina e ha mostrato che la CMC è diminuita quando la lunghezza della catena del carbonio nella catena idrofobica è stata aumentata da 10 a 12. L'aumento della lunghezza della catena di carbonio a 14 ha comportato un aumento della CMC, il che ha confermato che i tensiottanti gemini a catena lunga hanno una tendenza inferiore ad aggregare.
Faustino et al. ha riportato la formazione di micelle miste in soluzioni acquose di tensioattivi di gemelli anionici basati sulla cistina. I tensioattivi Gemelli sono stati anche confrontati con i corrispondenti tensioattivi monomerici convenzionali (C 8 CYS). I valori CMC delle miscele di superfattante lipidico sono stati riportati più bassi di quelli dei tensioattivi puri. I tensioattivi di gemelli e 1,2-dheptanoyl-sn-gliceryl-3-fosfocolina, un fosfolipide a forma di micelle e solubili in micelle, avevano CMC a livello millimolare.
Shrestha e Aramaki hanno studiato la formazione di micelle viscoelastiche simili a vermi in soluzioni acquose di tensioattivi anionici-nononici a base di aminoacidi misti in assenza di sali di miscela. In questo studio, è stato scoperto che il glutammato n-dodecile ha una temperatura di Krafft più elevata; Tuttavia, se neutralizzato con l'amminoacido di base L-lisina, ha generato micelle e la soluzione ha iniziato a comportarsi come un fluido newtoniano a 25 ° C.
6.2 Buona solubilità dell'acqua
La buona solubilità dell'acqua di AAS è dovuta alla presenza di ulteriori legami di co-NH. Ciò rende AAS più biodegradabile e rispettoso dell'ambiente rispetto ai corrispondenti tensioattivi convenzionali. La solubilità dell'acqua dell'acido N-acil-L-glutamico è ancora migliore a causa dei suoi 2 gruppi carbossilici. La solubilità idrica di CN (Ca) 2 è anche buona perché ci sono 2 gruppi di arginina ionica in 1 molecola, che si traduce in un adsorbimento e diffusione più efficaci all'interfaccia cellulare e persino un'inibizione batterica efficace a concentrazioni più basse.
6.3 Krafft Temperation e Krafft Point
La temperatura di Krafft può essere intesa come il comportamento specifico di solubilità dei tensioattivi la cui solubilità aumenta nettamente al di sopra di una particolare temperatura. I tensioattivi ionici hanno la tendenza a generare idrati solidi, che possono precipitare fuori dall'acqua. A una temperatura particolare (la cosiddetta temperatura di Krafft), di solito si osserva un aumento drammatico e discontinuo della solubilità dei tensioattivi. Il punto Krafft di un tensioattivo ionico è la sua temperatura di Krafft a CMC.
Questa caratteristica di solubilità è generalmente vista per i tensioattivi ionici e può essere spiegata come segue: la solubilità del monomero libero da tensioattivo è limitata al di sotto della temperatura di Krafft fino al raggiungimento del punto di Krafft, dove la sua solubilità aumenta gradualmente a causa della formazione di micelle. Per garantire la completa solubilità, è necessario preparare formulazioni di tensioattivi a temperature sopra il punto di Krafft.
La temperatura di Krafft di AAS è stata studiata e confrontata con quella dei tensioattivi sintetici convenzionali. Shrestha e Aramaki hanno studiato la temperatura di Krafft di AAS a base di arginina e hanno scoperto che la concentrazione critica di micelle ha mostrato un comportamento di aggregazione nella forma di n-zele di n-× AAS e ha discusso della relazione tra la temperatura di Krafft e i residui di aminoacidi.
Negli esperimenti, è stato scoperto che la temperatura di Krafft di N-hexadecanoyl AAS è aumentata con la riduzione delle dimensioni dei residui di aminoacidi (la fenilalanina essendo un'eccezione), mentre il calore della solubilità (assorbimento di calore) è aumentato con la riduzione delle dimensioni dei residui di aminoacidi (ad eccezione della glicina e della fenilalanina). Si è concluso che in entrambi i sistemi di alanina e fenilalanina, l'interazione DL è più forte dell'interazione LL nella forma solida del sale N-Hexadecanoyl AAS.
Brito et al. determinato la temperatura di Krafft di tre serie di nuovi tensioattivi a base di aminoacidi utilizzando microcalorimetria a scansione differenziale e ha scoperto che il cambiamento dello ione trifluoroacetato in ione ioduro ha comportato un aumento significativo della temperatura di Krafft (circa 6 ° C), da 47 ° C a 53 ° C. La presenza di legami cis-doppi e l'insaturazione presenti nei derivati ser-a catena lunga hanno portato a una significativa riduzione della temperatura di Krafft. È stato segnalato che il glutammato N-dodecile ha una temperatura di Krafft più elevata. Tuttavia, la neutralizzazione con l'amminoacido di base L-lisina ha portato alla formazione di micelle in soluzione che si comportava come fluidi newtoniani a 25 ° C.
6.4 Tensione superficiale
La tensione superficiale dei tensioattivi è correlata alla lunghezza della catena della parte idrofobica. Zhang et al. ha determinato la tensione superficiale del glicinato di cocoilo di sodio per metodo della piastra Wilhelmy (25 ± 0,2) ° C e ha determinato il valore della tensione superficiale a CMC come 33 mn -M -1, CMC come 0,21 mmol -L -1. Yoshimura et al. ha determinato la tensione superficiale della tensione superficiale a base di aminoacidi a base di aminoacidi di tipo N CYS di Agenti di superficie a base di N CYS. È stato scoperto che la tensione superficiale a CMC è diminuita con l'aumentare della lunghezza della catena (fino a n = 8), mentre la tendenza è stata invertita per i tensioattivi con lunghezze della catena n = 12 o più lunghe.
È stato anche studiato l'effetto di CAC1 2 sulla tensione superficiale dei tensioattivi a base di aminoacidi dicarbossilati. In questi studi, CAC1 2 è stato aggiunto a soluzioni acquose di tre tensioattivi di tipo di aminoacido dicarbossilato (C12 Malna 2, C12 Aspna 2 e C12 Gluna 2). I valori dell'altopiano dopo CMC sono stati confrontati e si è scoperto che la tensione superficiale è diminuita a concentrazioni di Cac1 2 molto basse. Ciò è dovuto all'effetto degli ioni di calcio sulla disposizione del tensioattivo all'interfaccia a gas. Le tensioni superficiali dei sali di N-dodecilaminomalonato e N-dodecilaspartato, d'altra parte, erano anche quasi costanti fino a 10 mmol-L -1 concentrazione di Cac1 2. Al di sopra di 10 mmol -L -1, la tensione superficiale aumenta bruscamente, a causa della formazione di una precipitazione del sale di calcio del tensioattivo. Per il sale disodio del glutammato N-dodecile, una moderata aggiunta di CAC1 2 ha comportato una significativa riduzione della tensione superficiale, mentre l'aumento continua della concentrazione di CAC1 2 non ha più causato cambiamenti significativi.
Per determinare la cinetica di adsorbimento degli AA di tipo gemini all'interfaccia a gas, la tensione della superficie dinamica è stata determinata usando il metodo massimo di pressione delle bolle. I risultati hanno mostrato che per il tempo di prova più lungo, la tensione dinamica dinamica 2C Cys non è cambiata. La diminuzione della tensione della superficie dinamica dipende solo dalla concentrazione, dalla lunghezza delle code idrofobiche e dal numero di code idrofobiche. L'aumento della concentrazione di tensioattivo, la riduzione della lunghezza della catena e il numero di catene hanno comportato un decadimento più rapido. I risultati ottenuti per concentrazioni più elevate di C n Cys (n = 8 a 12) sono risultati molto vicini al CMC γ misurato con il metodo Wilhelmy.
In un altro studio, le tensioni dinamiche di superficie della cistina di dilauril di sodio (SDLC) e del didecamino cistina di sodio sono state determinate con il metodo della piastra di Wilhelmy e, inoltre, le tensioni superficiali di equilibrio delle loro soluzioni acquose sono state determinate con il metodo del volume di caduta. La reazione dei legami disolfuro è stata ulteriormente studiata anche con altri metodi. L'aggiunta di mercaptoetanolo a 0,1 mmol -L -1SDLC ha portato a un rapido aumento della tensione superficiale da 34 mn -M -1 a 53 mn -M -1. Poiché il NACLO può ossidare i legami disolfuro di SDLC a gruppi di acido solfonico, non sono stati osservati aggregati quando il NaCLO (5 mmol -L -1) è stato aggiunto alla soluzione SDLC 0,1 mmol -L -1. La microscopia elettronica a trasmissione e i risultati di scattering dinamico della luce hanno mostrato che nella soluzione non sono stati formati aggregati. Si è scoperto che la tensione superficiale di SDLC aumenta da 34 mn -M -1 a 60 mn -M -1 per un periodo di 20 minuti.
6.5 Interazioni binarie di superficie
Nelle scienze della vita, un certo numero di gruppi ha studiato le proprietà vibrazionali delle miscele di AAS cationici (tensioattivi a base di arginina diacilglicerolo) e fosfolipidi all'interfaccia a gas-acqua, concludendo infine che questa proprietà non ideale provoca la prevalenza delle interazioni elettrostatiche.
6.6 Proprietà di aggregazione
La dispersione della luce dinamica è comunemente usata per determinare le proprietà di aggregazione di monomeri a base di aminoacidi e tensioattivi di gemelli a concentrazioni al di sopra della CMC, producendo un diametro idrodinamico apparente DH (= 2R H). Gli aggregati formati da C N CYS e 2cn CYS sono relativamente grandi e hanno una distribuzione su larga scala rispetto ad altri tensioattivi. Tutti i tensioattivi tranne 2c 12 CYS in genere formano aggregati di circa 10 nm. Le dimensioni delle micelle dei tensioattivi di gemelli sono significativamente più grandi di quelle delle loro controparti monomeriche. Un aumento della lunghezza della catena di idrocarburi porta anche ad un aumento della dimensione della micella. Ohta et al. ha descritto le proprietà di aggregazione di tre diversi stereoisomeri di n-dodecil-fenil-alanil-fenil-alanina tetrametilammonio in soluzione acquosa e hanno mostrato che i diastereoisomeri hanno la stessa concentrazione di aggregazione critica in soluzione acquosa. Iwahashi et al. Studiato dal dicroismo circolare, osmometria della pressione di vapore NMR e la formazione di aggregati chirali di acido N-dodecanoyl-L-glutamico, N-dodecanoyl-L-valine e i loro metilici di rotami di. per dicroismo circolare, osmometria a pressione di vapore e vapore.
6.7 Adsorbimento interfacciale
L'adsorbimento interfacciale di tensioattivi a base di aminoacidi e il suo confronto con la sua controparte convenzionale è anche una delle direzioni di ricerca. Ad esempio, sono state studiate le proprietà di adsorbimento interfacciale degli esteri dodecili di aminoacidi aromatici ottenuti da Let e LEP. I risultati hanno mostrato che Let e LEP hanno mostrato aree interfacciali più basse all'interfaccia gas-liquid e all'interfaccia acqua/esano, rispettivamente.
Bordes et al. ha studiato il comportamento della soluzione e l'adsorbimento nell'interfaccia di acqua a gas di tre tensioattivi di aminoacidi dicarbossilati, i sali di disodio di dodecil glutammato, aspartato dodecile e aminomalonato (con 3, 2 e 1 atomi di carbonio tra i due gruppi carbossilici, rispettivamente). Secondo questo rapporto, il CMC dei tensioattivi dicarbossilati era 4-5 volte superiore a quello del sale dodecilico monocarbossilato. Ciò è attribuito alla formazione di legami idrogeno tra i tensioattivi dicarbossilati e le molecole vicine attraverso i gruppi di ammide in essa.
6.8 Comportamento di fase
Le fasi cubiche discontinue isotropiche sono osservate per i tensioattivi a concentrazioni molto elevate. Le molecole di tensioattivo con gruppi di testa molto grandi tendono a formare aggregati di curvatura positiva più piccola. Marques et al. studiato il comportamento di fase dei sistemi 12 LYS12/12SER e 8LYS8/16SER (vedi Figura 10), e i risultati hanno mostrato che il sistema 12 LYS12/12SER ha una zona di separazione di fase tra le regioni micellari e vescicolari a micella, tra le regioni micellate a micella, tra le regioni di fase di micella emessa tra i piccoli micellari elaborati in fase di micella ettanta regione di fase). Va notato che per la regione della vescicola del sistema 12 LYS12/12SER, le vescicole sono sempre coesistenti con le micelle, mentre la regione delle vescicole del sistema 8LYS8/16SER ha solo le vescicole.
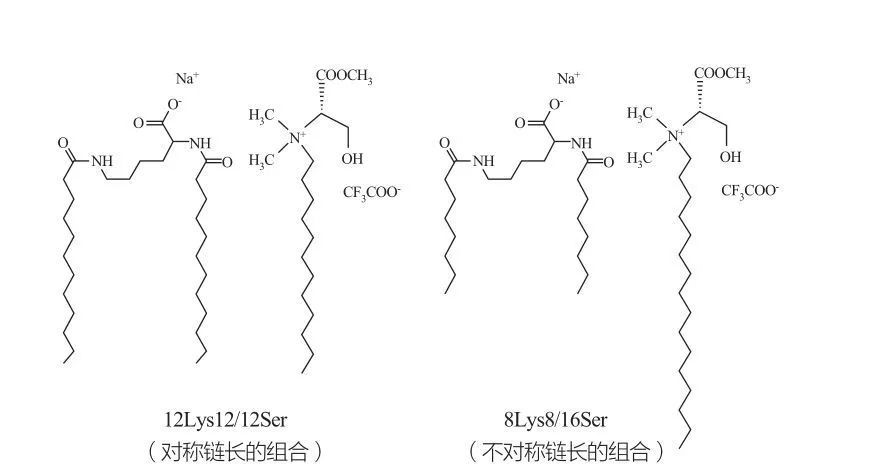
Miscele catanioniche dei tensioattivi a base di lisina e serina: coppia simmetrica 12lys12/12ser (a sinistra) e coppia asimmetrica 8LYS8/16ser (a destra)
6.9 Capacità emulsionante
Kouchi et al. ha esaminato la capacità di emulsionamento, la tensione interfacciale, la dispersibilità e la viscosità di N- [3-dodecil-2-idrossipropil] -L-arginina, L-glutammato e altri AA. In confronto ai tensioattivi sintetici (le loro controparti convenzionali non ioniche e anfoteriche), i risultati hanno mostrato che gli AA hanno una maggiore capacità emulsionante rispetto ai tensioattivi convenzionali.
Baczko et al. Nuovi tensioattivi anionici di aminoacidi anionici sintetizzati e studiato la loro idoneità come solventi della spettroscopia NMR orientati a chirale. Una serie di derivati L-PHE anfifilici a base di solfonati o L-Ala con diverse code idrofobiche (pentil ~ tetradecil) sono state sintetizzate reagendo gli aminoacidi con anidride O-solfobenzoica. Wu et al. sali di sodio sintetizzati di acile N-grasso e AAS eha studiato la loro capacità di emulsificazione nelle emulsioni petrolifere in acqua e i risultati hanno mostrato che questi tensioattivi si sono comportati meglio con l'acetato di etil come fase olio che con n-esano come fase petrolifera.
6.10 progressi nella sintesi e nella produzione
La resistenza all'acqua dura può essere intesa come la capacità dei tensioattivi di resistere alla presenza di ioni come calcio e magnesio in acqua dura, cioè la capacità di evitare le precipitazioni nei saponi di calcio. I tensioattivi con elevata resistenza all'acqua dura sono molto utili per formulazioni di detergenti e prodotti per la cura personale. La resistenza all'acqua dura può essere valutata calcolando la variazione della solubilità e dell'attività superficiale del tensioattivo in presenza di ioni di calcio.
Un altro modo per valutare la resistenza all'acqua dura è calcolare la percentuale o i grammi dei tensioattivi richiesti per il sapone di calcio formato da 100 g di oleato di sodio da dispersi in acqua. Nelle aree con alta acqua dura, alte concentrazioni di ioni calcio e di magnesio e contenuto minerale possono rendere difficili alcune applicazioni pratiche. Spesso lo ione di sodio viene usato come contro ione di un tensioattivo anionico sintetico. Poiché lo ione di calcio bivalente è legato a entrambe le molecole di tensioattivo, fa sì che il tensioattivo precipitasse più facilmente dalla soluzione che rende meno probabile la determinazione.
Lo studio della resistenza all'acqua dura degli AA ha mostrato che la resistenza all'acido e dell'acqua dura era fortemente influenzata da un ulteriore gruppo carbossilico e la resistenza all'acido e all'acqua dura è aumentata ulteriormente con l'aumento della lunghezza del gruppo distanziatore tra i due gruppi carbossilici. L'ordine di resistenza all'acido e dell'acqua dura era C 12 glicinato <c 12 aspartato <c 12 glutammato. Confrontando il legame ammidico dicarbossilato e il tensioattivo di amino dicarbossilato, rispettivamente, si è scoperto che l'intervallo di pH di quest'ultimo era più ampia e la sua attività superficiale è aumentata con l'aggiunta di una quantità adeguata di acido. Gli aminoacidi N-alchil dicarbossilati hanno mostrato un effetto chelante in presenza di ioni di calcio e un gel bianco formato C 12 C 12. Il glutammato C 12 ha mostrato un'elevata attività superficiale ad alta concentrazione di Ca 2+ e dovrebbe essere utilizzato nella desalinizzazione dell'acqua di mare.
6.11 Dispersibilità
La dispersibilità si riferisce alla capacità di un tensioattivo di prevenire la coalescenza e la sedimentazione del tensioattivo in soluzione.La dispersibilità è un'importante proprietà dei tensioattivi che li rende adatti all'uso in detergenti, cosmetici e prodotti farmaceutici.Un agente disperso deve contenere un estere, un etere, un legame ammino o un gruppo idrofobico e il gruppo idrofilo terminale (o tra i gruppi idrofobici a catena dritta).
In generale, i tensioattivi anionici come alcanolamido solfati e tensioattivi anfoterici come amidosulfobetaine sono particolarmente efficaci come agenti dispersi per i saponi di calcio.
Molti sforzi di ricerca hanno determinato la dispersibilità di AAS, in cui la lisina N-lauroil è risultata scarsamente compatibile con l'acqua e difficile da usare per le formulazioni cosmetiche.In questa serie, gli aminoacidi di base sostituiti da N-acil hanno una superba dispersibilità e vengono utilizzati nell'industria cosmetica per migliorare le formulazioni.
07 tossicità
I tensioattivi convenzionali, in particolare i tensioattivi cationici, sono altamente tossici per gli organismi acquatici. La loro tossicità acuta è dovuta al fenomeno dell'interazione con ioni di adsorbimento dei tensioattivi nell'interfaccia delle acque cellulari. La riduzione della CMC dei tensioattivi di solito porta a un adsorbimento interfacciale più forte dei tensioattivi, che di solito si traduce nella loro elevata tossicità acuta. Un aumento della lunghezza della catena idrofobica di tensioattivi porta anche ad un aumento della tossicità acuta del tensioattivo.La maggior parte degli AA sono bassi o non tossici per l'uomo e l'ambiente (specialmente per gli organismi marini) e sono adatti per l'uso come ingredienti alimentari, prodotti farmaceutici e cosmetici.Molti ricercatori hanno dimostrato che i tensioattivi di aminoacidi sono delicati e non irritanti per la pelle. I tensioattivi a base di arginina sono noti per essere meno tossici delle loro controparti convenzionali.
Brito et al. ha studiato le proprietà fisico-chimiche e tossicologiche degli anfifili a base di aminoacidi e i loro [derivati dalla tirosina (Tyr), idrossiprolina (HYP), serina (Ser) e lisina (LYS)] formazione spontanea di vescicole cationiche e hanno dato dati sulla loro tossica acuta a dafnia (Ic 50). Hanno sintetizzato le vescicole cationiche di bromuro di dodeciltrimetilammonio (DTAB)/Lys-Derivatives e/o miscele derivative di ser-/lys e hanno testato il loro dtab ecolitico, dimostrando che tutte le miscele AAS e le loro miscele che contengono le vescicole.
Rosa et al. ha studiato il legame (associazione) del DNA a vescicole cationiche stabili a base di aminoacidi. A differenza dei tensioattivi cationici convenzionali, che spesso sembrano essere tossici, l'interazione dei tensioattivi di aminoacidi cationici sembra essere non tossica. L'AAS cationico si basa sull'arginina, che forma spontaneamente vescicole stabili in combinazione con alcuni tensioattivi anionici. Anche gli inibitori della corrosione a base di aminoacidi sono riportati non-tossici. Questi tensioattivi sono facilmente sintetizzati con elevata purezza (fino al 99%), a basso costo, facilmente biodegradabili e completamente solubili nei media acquosi. Diversi studi hanno dimostrato che i tensioattivi di aminoacidi contenenti zolfo sono superiori nell'inibizione della corrosione.
In un recente studio, Perinelli et al. ha riportato un profilo tossicologico soddisfacente dei ramnolipidi rispetto ai tensioattivi convenzionali. È noto che i ramnolipidi fungono da potenziatori di permeabilità. Hanno anche riportato l'effetto dei ramnolipidi sulla permeabilità epiteliale dei farmaci macromolecolari.
08 Attività antimicrobica
L'attività antimicrobica dei tensioattivi può essere valutata mediante la concentrazione inibitoria minima. L'attività antimicrobica dei tensioattivi a base di arginina è stata studiata in dettaglio. I batteri Gram-negativi sono risultati più resistenti ai tensioattivi a base di arginina rispetto ai batteri Gram-positivi. L'attività antimicrobica dei tensioattivi è generalmente aumentata dalla presenza di legami idrossilici, ciclopropani o insaturi all'interno delle catene aciliche. Castillo et al. ha mostrato che la lunghezza delle catene aciliche e la carica positiva determinano il valore HLB (equilibrio idrofilo-lipofilo) della molecola, e questi hanno un effetto sulla loro capacità di interrompere le membrane. Il metil estere Nα-acilarginina è un'altra importante classe di tensioattivi cationici con attività antimicrobica ad ampio spettro ed è prontamente biodegradabile e ha una tossicità bassa o nullo. Studi sull'interazione dei tensioattivi a base di ester con metilico con nα-acilarginina con 1,2-dipalmitoil-SN-propiltrioxil-3-fosforilcolina e 1,2-ditetradecanoyl-SN-propiltrioxil-3-fosforilcholina, membrane modello e con organismi viventi in presenza di assunzione di assunzione esterne di assunzioni esterne di supera di supera Antimicrobici I risultati hanno mostrato che i tensioattivi hanno una buona attività antibatterica.
09 Proprietà reologiche
Le proprietà reologiche dei tensioattivi svolgono un ruolo molto importante nel determinare e prevedere le loro applicazioni in diversi settori, tra cui cibo, prodotti farmaceutici, estrazione di petrolio, assistenza personale e prodotti per l'assistenza domiciliare. Sono stati condotti molti studi per discutere la relazione tra viscoelasticità dei tensioattivi di aminoacidi e CMC.
10 applicazioni nel settore cosmetico
Gli AA sono utilizzati nella formulazione di molti prodotti per la cura personale.Il glicinato N-Cocoil di potassio è risultata delicato sulla pelle e viene utilizzato nella pulizia del viso per rimuovere i fanghi e il trucco. L'acido N-acil-L-glutamico ha due gruppi carbossilici, il che lo rende più solubile in acqua. Tra questi AA, AAS basati su acidi grassi C 12 sono ampiamente utilizzati nella pulizia del viso per rimuovere i fanghi e il trucco. Gli AA con una catena C 18 sono usati come emulsionanti nei prodotti per la cura della pelle e sono noti i sali di n-lauril alanina per creare schiume cremose che non sono irritanti per la pelle e possono quindi essere utilizzate nella formulazione dei prodotti per la cura del bambino. Gli AA a base di N-lauryl usati nel dentifricio hanno una buona determinazione simile al sapone e all'efficacia di inibizione degli enzimi.
Negli ultimi decenni, la scelta dei tensioattivi per cosmetici, prodotti per la cura personale e prodotti farmaceutici si è concentrata su bassa tossicità, mitezza, dolcezza al tatto e alla sicurezza. I consumatori di questi prodotti sono profondamente consapevoli della potenziale irritazione, tossicità e fattori ambientali.
Oggi, gli AA sono usati per formulare molti shampoo, tinture per capelli e saponi da bagno grazie ai loro numerosi vantaggi per le loro controparti tradizionali nei cosmetici e nei prodotti per la cura della persona.I tensioattivi a base di proteine hanno proprietà desiderabili necessarie per i prodotti per la cura personale. Alcuni AA hanno capacità di formazione dei film, mentre altri hanno buone capacità di schiuma.
Gli aminoacidi sono importanti fattori idratanti che si verificano naturalmente nello strato corneo. Quando le cellule epidermiche muoiono, diventano parte dello strato corneo e le proteine intracellulari vengono gradualmente degradate agli aminoacidi. Questi aminoacidi vengono quindi trasportati ulteriormente nello strato corneo, dove assorbono sostanze grassi o grassi nello strato epidermico corneum, migliorando così l'elasticità della superficie della pelle. Circa il 50% del fattore idratante naturale nella pelle è composto da aminoacidi e pirrolidone.
Il collagene, un ingrediente cosmetico comune, contiene anche aminoacidi che mantengono la pelle morbida.I problemi della pelle come la rugosità e l'ottusità sono dovuti in gran parte alla mancanza di aminoacidi. Uno studio ha dimostrato che la miscelazione di un aminoacido con un unguento ha alleviato le ustioni della pelle e le aree colpite sono tornate al loro stato normale senza diventare cicatrici cheloidi.
Gli aminoacidi sono stati anche trovati molto utili nella cura delle cuticole danneggiate.I peli secchi e informe possono indicare una diminuzione della concentrazione di aminoacidi in uno strato gravemente danneggiato. Gli aminoacidi hanno la capacità di penetrare nella cuticola nell'albero dei capelli e assorbire l'umidità dalla pelle.Questa capacità di tensioattivi a base di aminoacidi li rende molto utili in shampoo, coloranti per capelli, ammorbidenti, balsami per capelli e la presenza di aminoacidi rende forti i capelli.
11 Applicazioni nei cosmetici di tutti i giorni
Attualmente, vi è una crescente domanda di formulazioni di detergenti a base di aminoacidi in tutto il mondo.È noto che AAS ha una migliore capacità di pulizia, capacità di schiuma e proprietà di ammorbidimento del tessuto, il che le rende adatte a detergenti domestici, shampoo, lavaggi del corpo e altre applicazioni.Un AA anfoterico derivato dall'acido aspartico è riportato come un detergente altamente efficace con proprietà chelanti. È stato scoperto che l'uso di ingredienti detergenti costituiti da n-alchil-β-aminoetossi, riduce l'irritazione della pelle. È stata segnalata una formulazione di detergente liquido costituito da N-cocoil-β-aminopropionato come un detergente efficace per le macchie di olio sulle superfici metalliche. Un tensioattivo di acido aminocarbossilico, C 14 Chohch 2 NHCH 2 Coona, ha anche dimostrato di avere una migliore determinazione e viene utilizzato per pulire i tessuti, i tappeti, i capelli, il vetro, ecc. È noto che il derivato dell'acido n-aceto-n-aceto-aceto, è noto per avere una buona capacità di complessazione e quindi dare una stabilità a gravibilità.
La preparazione di formulazioni di detergenti basate su Keigo e Tatsuya e Tatsuya sono stati segnalati da n- (acil-β-alanil)-β-alanina per la capacità e la stabilità, la facile rottura della schiuma e il buon ammorbidimento del tessuto. KAO ha sviluppato una formulazione di detergente basata su N-acil-1 -n-idrossi-β-alanina e ha riportato una bassa irritazione cutanea, un'elevata resistenza all'acqua e un'alta potenza di rimozione delle macchie.
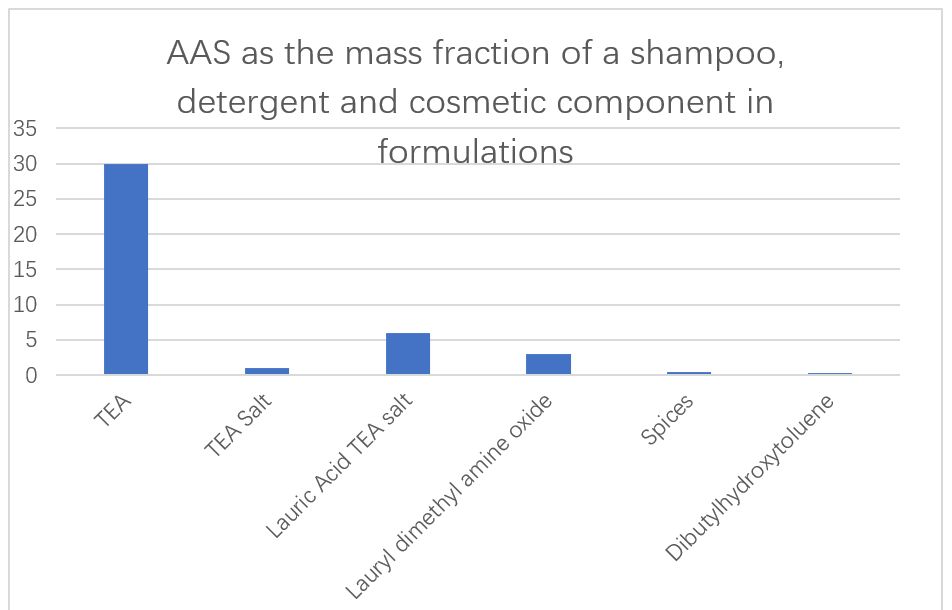
La società giapponese Ajinomoto utilizza AA a basso contenuto di tossico e facilmente degradabile basato su acido L-glutamico, L-arginina e l-lisina come ingredienti principali in shampoo, detergenti e cosmetici (Figura 13). È stata anche riportata la capacità degli additivi enzimatici nelle formulazioni di detergenti di rimuovere l'utilizzo delle proteine. N-acil AAS derivati da acido glutammico, alanina, metilglicina, serina e acido aspartico sono stati riportati per il loro uso come eccellenti detergenti liquidi in soluzioni acquose. Questi tensioattivi non aumentano affatto la viscosità, anche a temperature molto basse, e possono essere facilmente trasferiti dalla nave di conservazione del dispositivo di schiuma per ottenere schiume omogenee.
Tempo post: giugno-09-2022

